
医疗器械注册代办医疗器械康复训练床注册产品说明书和标签样稿如何编写?根据《康复训练床注册审查指导原则》相关要求,康复训练床产品的说明书和标签应符合《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局令第6号)、YY/T 0466.1、GB 9706.1、GB 24436、GB/T 26340和YY 9706.102中的相关要求。说明书、标签的内容应当真实、完整、科学,并与产品特性相一致,文字内容必须使用中文。说明书、标签中的文字、符号、图形、表格、数据等应相互一致,并符合相关标准和规范要求。
1.说明书除符合上述规定外,还应包括但不限于以下内容:
1.1产品特定人群使用的说明以及是否需要在医护人员的监护下使用的说明;
1.2产品技术要求的主要性能指标中明确需要在说明书中明示的内容;
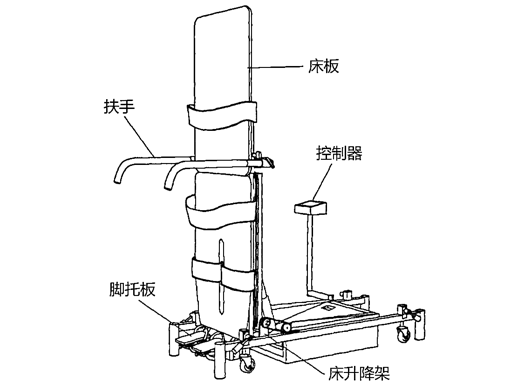
1.3完整的操作说明:产品的使用环境条件;安装及调试说明中应明确安装时对地面的要求;详细说明产品的具体使用方法及图示;
1.4应明确配件的更换方法及注意事项;应给出软件安装、升级等具体信息;
1.5若提供可由使用者更换或重新连接的固定装置,说明书中应说明验证固定装置是否已被可靠连接的方法;
1.6注意事项中至少应明确异常情况下,失控状态下的紧急处理措施。特殊情况下(停电、意外移动等)的注意事项,可能出现的误操作及可能造成的伤害;
1.7警告信息:例如在无人监护情况下禁止使用的警告,不当操作可能带来安全隐患的警告;
1.8安全工作载荷;
1.9整体尺寸和重量,包括主体部分的重量。
1.10申报产品附件的说明。
2.使用说明书审评关注点:
2.1应当提供拟申报范围内所有型号的说明书,应覆盖所申请的所有组成部分。
2.2产品名称、型号、规格、主要性能、结构与组成应与产品技术要求内容一致;产品的适用范围应与注册申请表、产品技术要求及临床评价资料一致。
2.3注册人/生产企业名称、住所、生产地址、联系方式及售后服务单位应真实有效,医疗器械注册人/生产企业名称和住所应与 《营业执照》一致;《医疗器械生产企业许可证》编号、医疗器械注册证书编号、产品技术要求编号位置应预留。
2.4与申报产品一起使用的其他医疗器械或不属于医疗器械的产品的描述,在说明书中应要求所连接设备应符合相应的 安全标准,并要求与该器械连接使用组成的系统所应符合相应的安全标准,及其他必要的信息。
医疗器械产品注册代办找深圳鸿远医疗器械咨询提供专业的技术服务!

 在线客服
在线客服